
近日,我校附二院运动医学科潘孝云课题组联合湖南大学史俊峰课题组在药学权威期刊Journal of Controlled Release(IF=10.8)发表了一篇题为“Enhancing calvarial defects repair with PDGF-BB mimetic peptide hydrogels”的研究论文。

在临床实践中,有效管理节段性骨缺损仍是一个巨大的挑战。尽管自体移植目前是治疗大量骨缺损的金标准,但其广泛使用受到供体短缺和相关发病率的影响。值得注意的是,约10%的患者存在与自体移植相关的并发症。因此,科学家和医生探索了各种方法,包括局部生长因子给药、基因治疗、干细胞递送以及骨组织工程的其他进展,所有这些都旨在促进骨再生。特别重要的是各种生长因子,包括血管内皮生长因子(VEGF)、胰岛素样生长因子(IGF)、成纤维细胞生长因子(FIGF)和血小板衍生生长因子(PDGF)在血管形成中起着关键作用,血管形成是骨折愈合和骨再生的关键方面。在这些生长因子中,PDGF在骨缺损修复方面得到了显著的认可。PDGF作为干细胞的强效有丝分裂原和化学引诱剂,有望促进骨再生。PDGF在骨损伤早期由血小板和巨噬细胞释放,不仅刺激局部血管生成,还协调成骨途径,加速骨快速再生。值得注意的是,重组PDGF-BB已获得FDA批准用于踝关节和后足的手术融合。
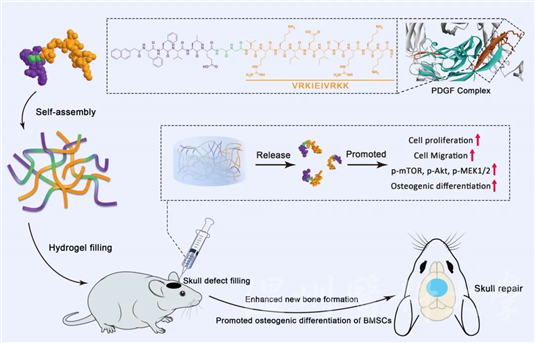
在这项工作中,我们引入了PDGF模拟肽(PMP1),与单体肽相比,其具有更高的活性和各种应用。我们之前的研究还表明,设计的PMP1可以自组装成富含原纤维的水凝胶,该水凝胶保持其生物学功能并表现出强大的稳定性。肽自组装成水凝胶主要由氢键、芳香族-芳香族相互作用和疏水相互作用驱动。因此,通过肽自组装形成的纳米纤维在体内暴露于伤口组织液时固有地具有分解成单体的能力。此外,降解肽的酶等因素促进了这种分解过程。这些酶诱导纳米纤维分解成单个单体,从而使它们能够从凝胶基质中释放出来。该研究不断优化模拟肽的设计合成并探索在促进大段骨缺损中的修复应用。研究发现PMP1自组装可以显著提升模拟肽的稳定性,并实现长时间的自缓释,可以促进细胞的增殖和迁移,增强成骨分化和钙沉积,显著地促进颅骨缺损的修复。
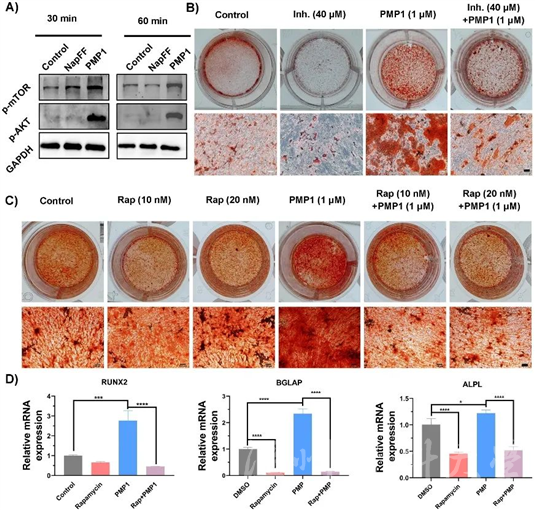
前期实验表明,该模拟肽在水溶液中能自组装形成超分子水凝胶,具有优良的生物稳定性。PMP1可以持久释放活性多肽,进而激活其生物学功能。进一步的分子机制研究表明PMP1激活PI3K-AKT-mTOR信号通路(A),这是其成骨作用的关键因素。通过成骨分化实验(B/C)和q-PCR分析,证明了PMP1增强骨髓间充质干细胞(BMSC)成骨分化的能力,显著增强关键成骨基因的表达增加(D);
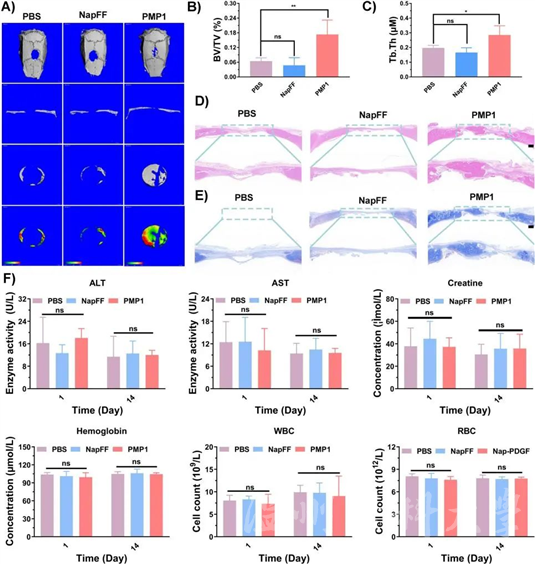
值得注意的是,在大鼠颅骨临界尺寸缺陷模型中,根据三维重建分析显示,与PBS和NapFF组相比,PMP1组的新生骨形成明显更大(A),对缺损区新形成骨与总组织(BV/TV)体积比以及骨小梁的厚度定量分析进一步验证了这一结果(B/C)。进一步使用H&E染色和Masson三色染色对颅骨骨缺损的组织学检查显示,与PBS组相比,PMP1组的矿化骨基质区域更完整(D/E)。以上结果说明了该模拟肽水凝可以显著促进颅骨缺损的修复。
温州医科大学附属第二医院潘孝云副教授和湖南大学袁丹副教授,史俊峰教授为共同通讯作者。据悉,该活性肽申请的专利已经授权。
扫一扫在手机打开当前页