
近日,药学院李校堃院士团队黄志锋课题组联合温医大附属第一医院陈永平团队在国际肝脏病学权威期刊Hepatology在线发表最新研究成果,阐明FGF4是一种肝脏内源性保护因子及非酒精性脂肪肝疾病(NAFLD/NASH)的新型生物标记物,并证明重组FGF4蛋白可显著遏制代谢性肝脏炎症进展及NASH相关肝纤维化的病理进展,为日益严峻的NAFLD/NASH提供了一种全新的诊疗分子和药物干预策略。这是团队继发现FGF4作用于骨骼肌发挥血糖调控作用后(Nat Commun, 2021; 12:51258)针对FGF4生物学功能的又一重要新发现。黄志锋教授,李校堃院士,陈永平教授为论文共同通讯作者,青年教师宋林涛和博士研究生王璐瑶、侯煜姝为共同第一作者。

非酒精性脂肪性肝病(NAFLD)是指排除酒精和其他明确的损肝因素,以弥漫性肝细胞大泡性脂肪变为主要病理表现,可影响全身多系统的遗传—代谢—病理临床综合征,其疾病发展谱极为广泛,包括可逆转的肝脂肪变性和非酒精性脂肪肝炎(NASH)以及后期不可逆的纤维化、肝硬化乃至最终的肝细胞癌(HCC)。近十年来,我国NAFLD的患病率高达20%以上,已取代慢性病毒性肝病跃居慢性肝病之首。但目前针对NAFLD/NASH的临床治疗手段和药物非常匮乏,亟需探明新的治疗靶点,研发新的治疗药物。
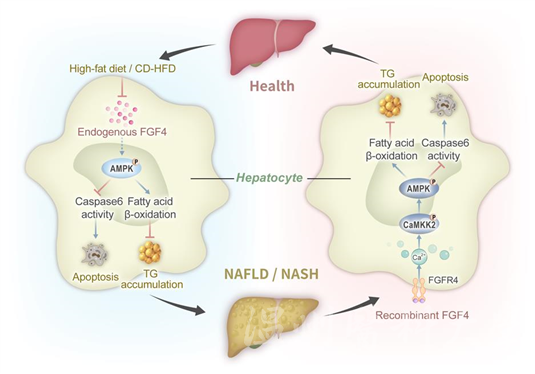
成纤维细胞生长因子(FGFs)是哺乳动物体内分布极为广泛的一类重要细胞因子,包括18个成员,它们以旁分泌或内分泌方式介导发育、组织内稳态/修复和机体代谢中许多关键事件。近年来研究发现FGFs家族多个成员参与维持肝脏组织细胞和代谢的稳态。为探索FGFs是否在NAFLD/NASH进展中发挥调控作用,本研究首先通过大样本临床分析发现肝实质细胞特异表达的FGF4是FGFs家族成员中唯一的NAFLD/NASH负性响应因子,与脂肪肝病人的病程进展呈现显著的负相关,进一步通过构建肝脏实质细胞特异性敲除Fgf4的转基因老鼠以及HFD诱导的NAFLD和胆碱缺乏的HFD(CD-HFD)诱导的NASH小鼠模型,发现外源重组rFGF4能够显著减轻NAFLD/NASH小鼠肝脏脂肪变性、炎症、肝脏损伤和纤维化,从而达到改善甚至逆转NAFLD/NASH的作用。研究从病理、生理和药理三个维度阐释了FGF4是NAFLD/NASH的全新潜在治疗靶点和候选药物分子,证实了FGF4可通过激活肝细胞特异性受体FGFR4而促进钙离子内流,进而激活CaMKK2-AMPK-Caspas6通路,从而抑制肝细胞凋亡、改善肝脏脂质堆积,显著遏制炎症进展,并且具有更好的药物安全性。
论文链接:https://aasldpubs.onlinelibrary.wiley.com/doi/abs/10.1002/hep.32404
扫一扫在手机打开当前页